CelloVie标准化iPSC分化流程的人源脊髓运动神经元,具备高纯度,并稳定表达ISL1、SMI32、HOXB4等运动神经元的典型标志物,能够有效模拟人类脊髓运动神经元的关键形态学与功能性特征。细胞展现出良好的轴突延伸、神经网络形成及体外存活能力。凭借其高度一致性与可靠性,该细胞模型可广泛应用于肌萎缩侧索硬化症(ALS)、脊髓性肌萎缩症(SMA)等神经退行性疾病的体外建模、药物测试及病理机制探索。
细胞共表达运动神经元标志物ISL1(红色)和成熟轴突标志物SMI32(绿色)。细胞呈现复杂的神经突网络结构,反映其在形态与功能上的成熟性,适用于神经疾病建模、电生理研究与药物筛选等多种应用。
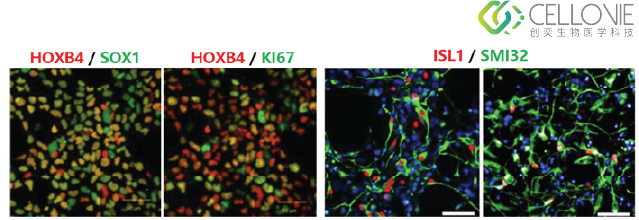
图:运动神经元分化展现出典型标志物表达特征
CelloVie分化生成的运动神经元在不同阶段的免疫染色结果。早期细胞共表达HOXB4与神经祖细胞标志物SOX1及增殖标志物KI67,表明其具备后轴向神经祖细胞特性;后期细胞表达运动神经元标志物ISL1与成熟轴突标志物SMI32,验证其成功向功能性运动神经元分化。
技术特性与优势
● 关键标志物的稳定表达:高表达HOXB4、ISL1与SMI32等典型分子。
● 成熟的神经元功能:具备典型的神经元形态、活跃的突起延伸能力以及形成功能性轴突网络。
● 模型一致性强:不同批次细胞分化表现稳定,适合长期项目需求。
● 人源化模型:提供更贴近人类生理病理状态的体外研究工具,有助于提高临床转化潜力。
● 适配多种实验平台:兼容功能成像、电生理与高通量筛选系统。
● 支持疾病建模与突变验证:适用于多种基因背景与临床突变建模。
主要应用领域
● 疾病建模:构建肌萎缩侧索硬化症(ALS)、脊髓性肌萎缩症(SMA)等运动神经元退行性疾病的人源化体外模型。
● 基因功能研究:评估特定基因突变(如SOD1、TDP43、FUS、C9orf72 等)对神经元存活、形态及功能的影响。
● 病理机制探索:研究轴突生长与退化、细胞应激反应、蛋白聚集及神经毒性等病理过程。
● 药物筛选与验证:用于神经保护性化合物的筛选、有效性评估及作用机制研究。
● 神经肌肉连接研究:可与肌肉细胞共培养,用于构建和研究运动神经-肌肉连接。